Chimie Organique
Molecules Organiques
et Médicinales
Des planches
BD
Les Aromatiques
© The scientific sentence. 2010
| |
|
Chimie organique : Les hydrocarbures
Les hydrocarbures saturés
1. Les hydrocarbures saturés: Les alcanes
Les atomes de carbone sont tétravalents. Ils
peuvent former 4 liaisons avec autres atomes.
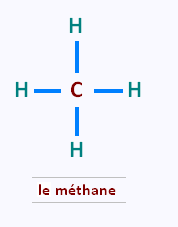
Lorsqu'un atome de carbone se lie à 4 atomes d’hydrogène, il
forme la molécule de méthane de formule brute CH4.
Sa formule développée est la suivante:
L'atome de carbone forme 4 liaisons simples avec
4 atomes d'hydrogène.
Un hydrocarbure possède la propriété d'être saturé lorsqu'il
est lié à un maximum possible d'atomes d’hydrogène
.
Ainsi, un hydrocarbure qui présente cette propriété est dit saturé.
Ces hydrocarbures saturés sont appelés des alcanes. Ils
sont nommés par le préfixe alc suivi de ane. Le plus simple est le
méthane.
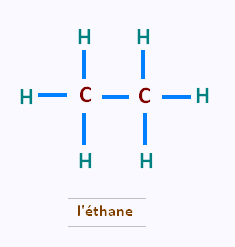
Le second alcane est l’ éthane de formule brute C2H6.
Sa formule développée est représenté ci-contre.
Les deux carbones forment une simple liaison entre eux
et entre les hydrogènes. On note que cet hydrocarbure est saturé.
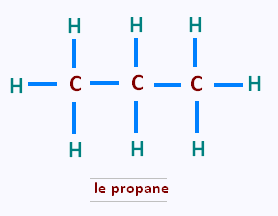
Le suivant est le propane de formule brute C3H8.
Sa formule développée est représenté ci-contre.
Dans le cas général, la formule brute d'un alcane est
CnH2(n+1)
1. Les alcanes les plus simples
Voici la liste des alcanes le plus courants:
| Alcanes |
| nom | formule |
|---|
| méthane | CH4 |
| éthane | C2H6 |
| propane | C3H8 |
| butane | C4H10 |
| pentane | C5H12 |
| hexane | C6H14 |
| heptane | C7H16 |
| octane | C8H18 |
| nonane | C9H20 |
| décane | C10H22 |
| pentadécane | C15H32 |
| eicosane | C20H42 |
|
|